Anvisa aprova segundo lote da vacina CoronaVac
Novo pedido aprovado se refere a doses do imunizante envasadas no Brasil
A Anvisa (Agência Nacional de Vigilância Sanitária) aprovou na tarde desta sexta-feira, 22, a autorização emergencial em caráter experimental do segundo lote com 4,8 milhões de doses da vacina CoronaVac, desenvolvida em pela farmacêutica chinesa Sinovac em parceria com o Instituto Butantan. A decisão da Diretoria Colegiada foi unânime.
A diferença da análise do segundo lote para o primeiro está no fato de que o envase e os processos de rotulagem e embalagem foram feitos pelo Instituto Butantan.
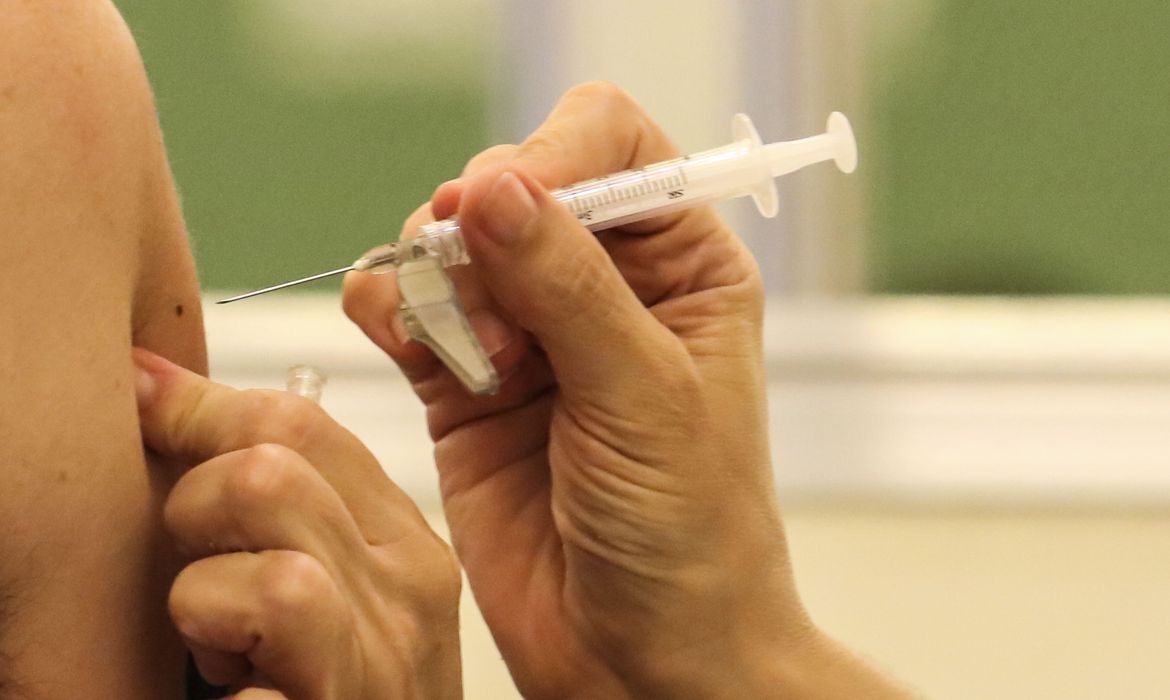
No último domingo, a agência já havia liberado o uso de 6 milhões de doses da CoronaVac.
- Valle del Elqui: o paraíso chileno ensolarado que une natureza, vinhos e astroturismo
- Microsoft abre curso gratuito para mulheres; saiba como se inscrever
- AVC: saiba como prevenir e identificar os sinais de alerta
- Senai oferta mais de 5 mil vagas em cursos gratuitos
De acordo com a Anvisa, as dez doses devem ser aplicadas no prazo de oito horas após o recipiente ser aberto. A agência alerta para o fato de que, passadas oito horas da abertura do frasco, não é possível garantir a integridade e a pureza da vacina.
As doses em frascos fechados, que nunca foram abertos, têm, segundo a Anvisa, prazo de validade de 12 meses, de acordo com as primeiras análises.
Ainda segundo a Anvisa, os frascos precisam ser armazenados em temperatura entre dois a oito graus, mas suportam, fora dessa temperatura, tempo suficiente para a aplicação nas pessoas.