Anvisa libera uso emergencial de sotrovimabe contra covid-19
Uso restrito do medicamento é a hospitais, sob prescrição médica e sua venda é proibida ao comércio
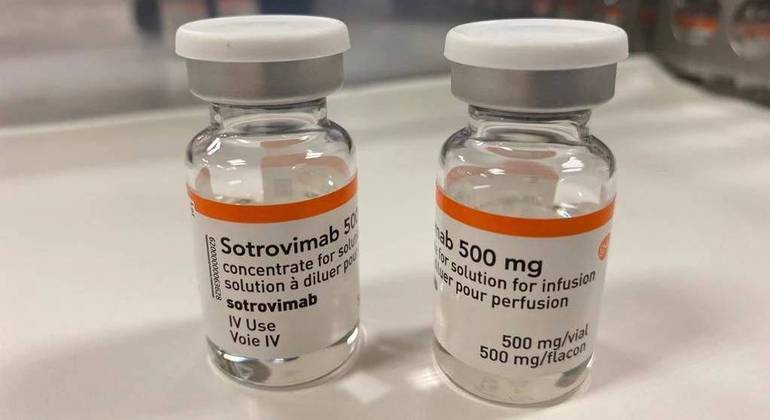
A Agência Nacional de Vigilância Sanitária (Anvisa) liberou nesta quarta-feira, 8, o uso emergencial de mais um anticorpo monoclonal para ser usado no tratamento de covid-19: o sotrovimabe.
O medicamento, desenvolvido pela farmacêutica britânica GsK (GlaxoSmithKline), destina-se a pacientes com quadros leves ou moderados de novo coronavírus e com risco de evoluir para formas mais graves da doença.
O sotrovimabe é indicado a idosos, imunossuprimidos, doentes pulmonares crônicos (incluindo asmáticos), portadores de diabetes mellitus tipos 1 ou 2, doentes renais crônicos (incluindo pessoas em diálise) e indivíduos com hepatite crônica.
- Olímpia é destino certa para férias em família no interior de SP
- Como manter o equilíbrio alimentar nas celebrações de fim de ano?
- A verdade sobre a vitamina C: entenda quando e como o excesso faz mal ao corpo
- Trem turístico vai ligar Rio de Janeiro e Minas Gerais
A aplicação é intravenosa, com dose única restrita 500 mg da droga e o tratamento deve ser iniciado após o teste positivo para a covid-19 e dentro de cinco dias do início dos sintomas.
A incorporação do sotrovimabe no Sistema Único de Saúde (SUS) depende da avaliação do Ministério da Saúde.
O uso do sotrovimabe é restrito a hospitais e a venda é proibida ao comércio.
Sotrovimabe não é recomendado em casos graves
A Anvisa alerta que o sotrovimabe não pode ser administrado em pacientes com quadros graves de covid-19 ou em uso de oxigenoterapia.
Segundo a agência, esse tipo de medicamento tem risco de piorar o estado de saúde de pacientes nessas condições.
Anvisa alerta ainda que o uso em mulheres grávidas deve ser feito com cautela, uma vez que há dados limitados do uso medicamento nessa população.
A FDA (Agência de Medicamentos e Alimentos dos EUA) e a EMA (Agência Europeia de Medicamentos) liberaram o uso emergencial do sotrovimabe em maio.