Anvisa autoriza compra dos insumos para produção da vacina chinesa
O instituto só poderá aplicar a vacina se obtiver registro da agência. Caso não ocorra, todo o produto deverá ser destruído
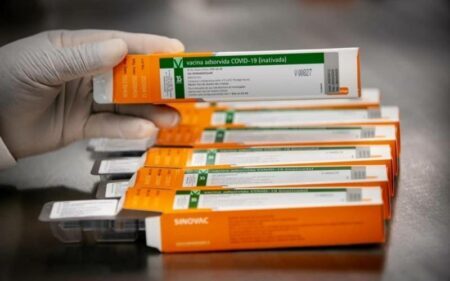
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta quarta-feira, 28, a importação de insumos chineses para fabricação, no Brasil, da CoronaVac, vacina contra a covid-19 desenvolvida pelo laboratório chinês Sinovac em parceria com o Instituto Butantan, de São Paulo. Por unanimidade, a diretoria da agência aprovou a importação de 120 bolsas com 200 litros cada do produto necessário.
“Essa era uma autorização que constava no processo que contemplava a vacina já pronta e também a matéria-prima. As vacinas já prontas já foram autorizadas e agora estamos autorizando a vinda para o Brasil de matéria-prima, que é claro terá todo o atesto de segurança do manuseio desse material assumido pelo próprio Instituto Butantan, que é claro tem condições para isso, para que possa ter o início os ajustes da fase de produção”, explicou o diretor-presidente da Agência Nacional de Vigilância Sanitária (Anvisa), o contra-almirante Antonio Barra Torres, em entrevista à CNN.
Apesar da autorização, a Anvisa impôs uma serie de condições ao Butantan para a compra da matéria-prima. O instituto será responsável pelo produto no Brasil e precisará seguir todas as normas de biossegurança. Além disso, ele só poderá aplicar a vacina se obtiver registro da Anvisa. Caso não ocorra, todo o produto deverá ser destruído.
- Terror noturno: 5 pontos que ajudam a explicar o transtorno
- Estudo aponta o suco que pode aumentar a capacidade do corpo de queimar gordura
- SP abre mais de 20 mil vagas para cursos gratuitos; veja como participar
- O que fazer em João Pessoa? Visite essas 3 praias de tirar o fôlego
A Anvisa levou mais de um mês para liberar a compra dos insumos, mesmo o Instituto Butantan tendo pedido urgência na questão. Desde a semana passada, o presidente do instituto, Dimas Covas, vem cobrando a agência. Nesta quarta-feira, ele falou sobre o atraso no cronograma da produção da CoronaVac, justamente por causa da demora da Anvisa em liberar a compra da matéria-prima.
Segundo Dimas Covas, o que era pra ter começado na segunda quinzena de outubro, agora, está previsto no mínimo para novembro. “Nossa previsão era iniciar a (fabricação da) vacina do Butantan na segunda quinzena de outubro. Foi solicitada para a Anvisa em 23 de setembro a autorização para importação da matéria-prima da China. Ainda não saiu. Esse atraso pode ter efeito na produção da vacina. Cada dia que aguardamos é um dia a menos de vacina”, havia afirmado o diretor do Instituto Butantan, horas antes da Avisa liberar a compra.
Segundo o diretor do Butantan, a fábrica do instituto está pronta para iniciar a produção da vacina, que só poderá ser aplicada na população, após autorização e registro da Anvisa. “O Butantan tem trabalhado em necessidade da urgência da situação e do momento, desde o início quando começamos o processo de vacina (…) Nossa fábrica está pronta e operacional, só aguardamos a autorização”, disse Dimas Covas.
Além da liberação de compra de insumos, a Anvisa também já autorizou a importação de 6 milhões de doses da CoronaVac, da China.
A liberação da importação de doses e insumos é parte importante do caminho, pois para a conclusão dos estudos e posterior submissão do registro na Anvisa, o Instituto Butantan precisa apresentar dados que comprovem a eficácia da vacina.
Para essa comprovação de eficácia, é preciso um número mínimo de voluntários infectados pelo coronavírus para comparação entre o grupo que tomou placebo e o grupo que recebeu a vacina em teste.
O presidente Jair Bolsonaro (sem partido) tem feito da vacina terreno de disputa com o governo do Estado de São Paulo, por sua rixa com João Doria (PSDB). Na última semana, Bolsonaro desautorizou a intenção de compra assinada pelo ministro da Saúde, Eduardo Pazuello, para uso da vacina pelo Sistema Único de Saúde (SUS).