Novo medicamento para psoríase é aprovado pela Anvisa
Tratamento pode melhorar em até 60% lesões na pele de pacientes adultos
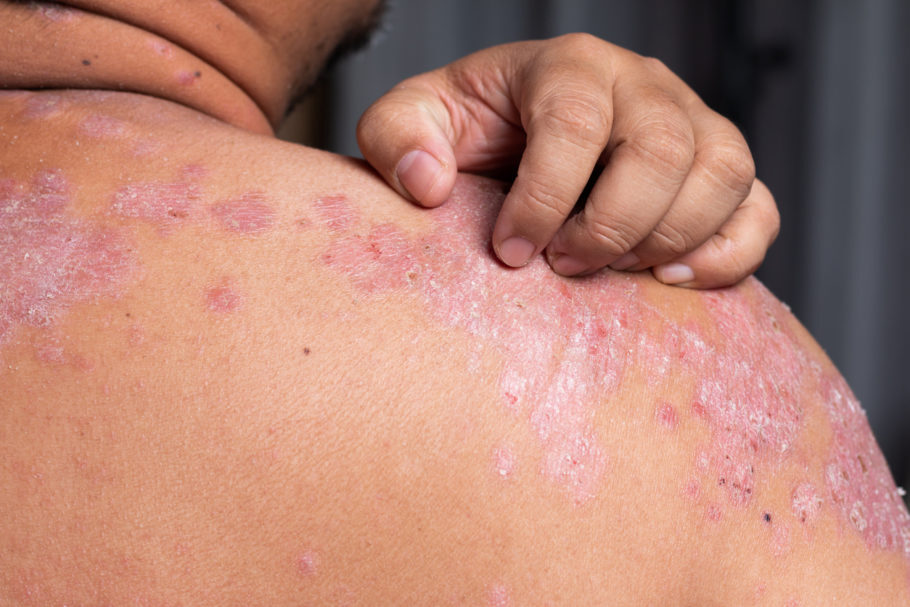
A Agência Nacional de Vigilância Sanitária (Anvisa) liberou um tratamento para psoríase que é a nova esperança para amenizar o problema na pele. Trata-se do SKYRIZI- risanquizumabe. De acordo com estudos clínicos, mais de 60% dos pacientes que usaram o medicamento apresentaram melhora completa das lesões em 52 semanas.
A aprovação foi publicada no Diário Oficial da União em 27 de maio de 2019.6
A indicação do remédio é para pacientes adultos com psoríase em placas em estágio de moderado a grave. A administração do SKYRIZI é via subcutânea e a dose recomendada é de 150mg, com prescrição médica.
No início do mês, a agência já havia liberado outros dois medicamentos para a doença: o Tremfya (guselcumabe), recomendado para adultos com lesões secas e escamas na pele em estágios de moderado a grave e o Otezla (apremilaste), indicado tratamento da artrite psoriásica ativa, também para pacientes adultos.
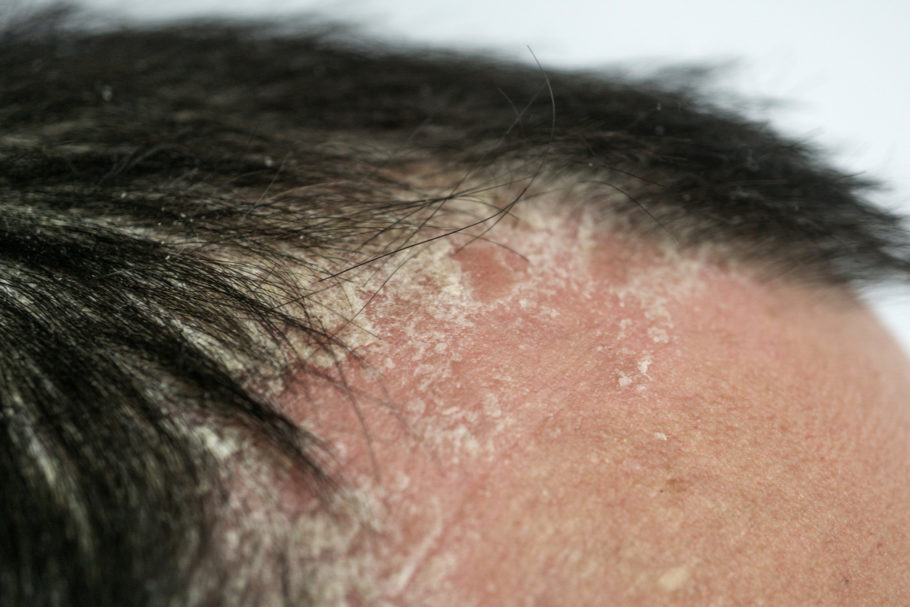
Psoríase
A psoríase é uma doença crônica que não tem cura. Carateriza-se por manchas rosas ou avermelhadas, cobertas por escamas esbranquiçadas. A doença não contagiosa e atinge homens e mulheres, em qualquer idade, podendo ocorrer desde formas localizadas e discretas, até formas muito severas que acometem grande área da superfície corporal.
Segundo a Sociedade Brasileira de Dermatologia, a psoríase causa lesões arredondadas, vermelhas e descamativas, que muitas vezes geram preconceito e diminuem a qualidade de vida dos pacientes acometidos.
Saiba mais sobre a doença, os tipos e tratamentos no link abaixo: